脑科学与智能技术卓越创新中心异位表达tbx2和atoh1诱导小鼠损伤模型的内毛细胞原位再生研究
文章来源:脑科学与智能技术卓越创新中心 | 发布时间:2023-12-12 | 【】 【】
2023年12月11日,《development》杂志在线发表了题为《》的研究论文。该研究由中国科学院脑科学与智能技术卓越创新中心(神经科学研究所)刘志勇研究组完成。研究团队构建了耳蜗内毛细胞特异性损伤的小鼠模型,并在该模型的基础上把幼年耳蜗支持细胞转分化为新的内毛细胞,从而实现了损伤耳蜗内源性内毛细胞后的原位再生,并对新的内毛细胞进行了全面详细的转录组学,形态学和电生理特性等分析。
耳蜗是听觉系统的第一级声音感受器,其内部的柯蒂氏器官有序排列着三排外毛细胞、一排内毛细胞及不同类型的支持细胞。内毛细胞负责将声波转换为电信号,并传递给螺旋神经节(听神经)。与非哺乳类动物(如鱼类和鸟类)不同,哺乳类动物丧失了再生毛细胞的能力,因此毛细胞一旦损坏将导致不可逆的永久性耳聋。ibcs/iphs是耳蜗支持细胞的两种亚型,它们与内毛细胞在空间位置上彼此相邻,并且在发育过程中具有相似的细胞起源。因此,ibcs/iphs是内毛细胞再生的潜在细胞来源和基因操纵靶点(图1a)。本实验室前期通过在新生小鼠耳蜗ibcs/iphs中条件性地异位过表达atoh1和tbx2,在正常(没有损伤)耳蜗内成功地将ibcs/iphs转分化为vglut3 新生内毛细胞。但仍有几个关键问题亟待解决:1)在内毛细胞损伤的耳蜗内,能否再生出新的内毛细胞?2)新的内毛细胞与野生型内毛细胞在转录组水平和电生理特性方面的相似度如何?3)新的内毛细胞能否实现听力的恢复或者部分恢复?
为解决以上科学问题,研究人员首先构建了内毛细胞特异性损伤的小鼠模型fgf8-dtr/ 小鼠模型。当fgf8-dtr/ 被注射白喉毒素(dt)后,可以导致97.8%的内毛细胞死亡。为了探究损伤野生型内毛细胞能否增加支持细胞转分化为内毛细胞的效率,研究人员构建了一个能够进行精细调控基因表达的小鼠模型,plp1-creer ;rosa26-loxp-stop-loxp-tbx2-p2a-dhfr*atoh1*dhfr-t2a-tdtomato/ ; fgf8-dtr/ (简称plp1-tat-dtr),并分为两组: 1)第一组作为对照组,仅在p2注射dt (图1b-b”和图2a-a’); 2)第二组在p0和p1注射他莫西芬 (tmx)﹑p2注射dt,p3和p4注射甲氧苄啶 (tmp, 用于结合dhfr,从而瞬时稳定atoh1的表达),被定义为tmx/dt/tmp实验组(图1c-c”和图2b-b’)。实验结果显示,实验组有477.0 48.0个内毛细胞,远远高于对照组(17.3 4.0)。并且损伤情况下的新生内毛细胞的再生效率(73.5% 2.3%)显著高于未损伤的再生效率(29.5% 1.2%,图1d)。更为重要的是,单细胞转录组分析(图1e)和膜片钳电生理分析(图1f-g)表明新的内毛细胞和野生型的内毛细胞具有高度的相似度(达60%以上),透射电镜可观察到新的内毛细胞囊泡结构的产生(图2c-d’)。本研究首次证明了当内源性内毛细胞受损时,新生ibcs/iphs中异位表达atoh1和tbx2,可以再生出新的内毛细胞,它们在转录组和电生理水平上,与内源性内毛细胞有60%以上的相似度,并且再生效率比没有内源性内毛细胞损伤时有显著提高。
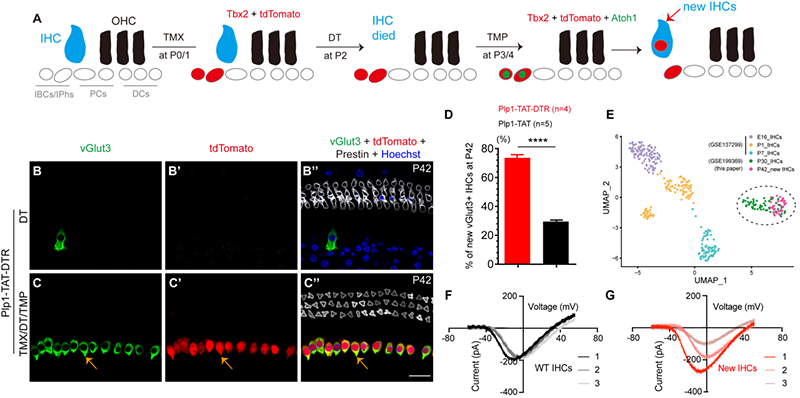
图1:a.内毛细胞损伤再生的示意图;b.内毛细胞损伤小鼠模型可以高效特异的损伤内毛细胞;c.在内毛细胞损伤的情况下,异位表达atoh1与tbx2可再生出vglut3 的新生内毛细胞;d.损伤情况下的再生毛细胞效率显著提高;e.转录组水平上,新生毛细胞与野生型p30内毛细胞聚为一群;f-g.新生内毛细胞的电压依赖的ca电流与野生型内毛细胞相似。
为了探讨再生出的新生内毛细胞是否具有生物学功能,研究人员通过听觉脑干反应检测并比较了plp1-ai9(tmx/tmp,阳性对照组)、plp1-tat-dtr(dt,阴性对照组)和plp1-tat-dtr(tmx/dt/tmp,实验组)三者之间的听力,结果显示实验组小鼠的听力未能得到恢复(图2e)。为了进一步寻找听力不能恢复的主要原因,研究人员利用电生理技术,发现新的内毛细胞不具备机械敏感电转导通道电流(图2f-h)。该发现解释了新的内毛细胞无法感知外界声音信号,无法恢复听力的原因,从而为未来如何再生出有功能的毛细胞提供了方向。
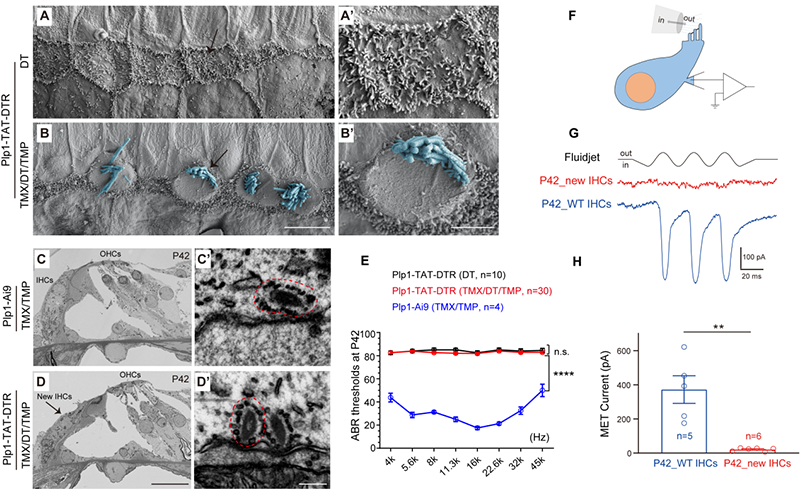
图2.a-b.扫描电镜可观察到在内源内毛细胞损伤的情况下,新生内毛细胞可再生出新的纤毛结构;c-d.透射电镜可观察到新生内毛细胞有囊泡结构的产生;e.但小鼠听力未能得到有效的改善;f-h.电生理技术发现新的内毛细胞不具备机械敏感的met通道电流。
中国科学院脑科学与智能技术卓越创新中心刘志勇研究员与毕政鸿副研究员为本论文的通讯作者,刘志勇组副研究员李响为本论文的第一作者,博士研究生任旻蕙在生物信息学分析上做了大量工作,博士研究生顾云鹏和研究助理朱彤为本项目做了重要贡献,上海交通大学第九人民医院张宇博士和脑智卓越中心李杰博士共同完成电生理研究内容,脑智卓越中心副研究员李超和王广琴博士也对本项目提供了帮助,上海交通大学第九人民医院宋雷教授对本课题电生理内容给予了重要的指导。中国科学院脑智卓越中心光学平台、电镜平台、分子细胞技术平台和啮齿类实验动物平台提供了重要j9九游会登录入口首页旧版的技术支持。该研究获得了国家自然科学基金委员会、科技部、上海市科委和中国科学院的资助。
